【东大新闻网12月4日电】(通讯员 陈早早)近日,东南大学公共卫生学院梁戈玉教授联合陈早早研究员团队在国际著名学术期刊《ACS Nano》在线发表题为“Unveiling the Heart’s Hidden Enemy: Dynamic Insights into Polystyrene Nanoplastic-Induced Cardiotoxicity Based on Cardiac Organoid-on-a-Chip” (揭开心脏隐藏的敌人:基于心脏类器官芯片动态观察聚苯乙烯纳米塑料诱导的心脏毒性) 的论著。该研究基于前沿医工交叉技术,构建了心脏类器官芯片(COoC)并开展了新型污染物——聚苯乙烯纳米塑料(PS-NPs)的心脏毒理学研究。
塑料产品在全球范围内无处不在,随着时间的推移,可逐渐分解成微塑料和纳米塑料。微纳米塑料(MNPs)广泛分布于生态系统中,目前已成为全球新型污染物。人体血液和多脏器中均被证实可以检测到微纳米塑料的存在,其潜在的健康效应不容忽视。
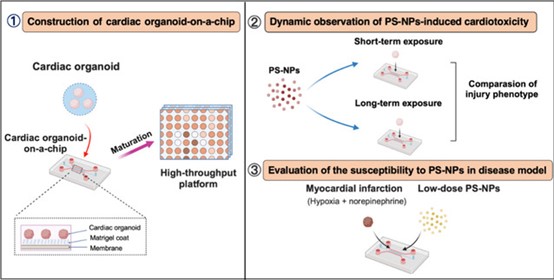
先前的研究已初步证明MNPs具有潜在的心脏毒性,但对其损伤效应及潜在机制仍缺乏更全面认知,主要受限于以下的原因:(1)当前研究严重依赖传统的毒理学平台,其种属差异以及体外2D模型缺失细胞通讯等不足影响了研究结论的可靠性。(2)目前的研究大多采取MNPs的单一时间点暴露,忽略了对不同暴露时间窗口下损伤事件的捕捉。(3)现有研究几乎都是基于健康模型评估MNPs的心脏损伤风险,在心脏病理条件下对于MNPs的易感性知之甚少。为解决上述限制,梁戈玉教授/陈早早研究员团队构建了包含有多种关键心脏细胞类型的人诱导多能干细胞(iPSC)衍生的心脏类器官(CO),并整合器官芯片技术(OoC),高仿真性地模拟了暴露场景,对短期和长期暴露于PS-NPs引起的心脏损伤进行了动态观察。其结果证实氧化应激、炎症应答、钙离子稳态失衡和线粒体功能障碍是触发心脏损伤的早期关键事件,心脏纤维化是长期暴露后的晚期结局。值得注意的是,尽管低剂量PS-NPs在健康模型中没有表现出明显的心脏毒性,但病理状态下加剧了心肌梗死症状。上述发现进一步加深了对于PS-NPs诱导的心脏毒性过程的理解,并提供了一个新型的体外心脏毒性评估平台,包含微流控系统和多细胞互作,为探究复杂的心脏病理生理学研究奠定基础。
东南大学公共卫生学院张天翊博士为该论文的第一作者,东南大学公共卫生学院梁戈玉教授与生物科学与医学工程学院陈早早研究员为该论文的共同通讯作者。该工作受到国家自然科学基金和江苏省前沿引领技术基础研究重大项目等资助。
论文链接:https://pubs.acs.org/doi/10.1021/acsnano.4c13262
供稿:公共卫生学院
(责任编辑:吴涵玉审核:李小男)

