【东大新闻网5月23日电】(通讯员 赵健)光动力疗法具有较高的时空选择性和微创性,对健康组织的副作用小,已成为一种有前景的癌症治疗新方法。但目前传统的光敏剂存在吸收波长短,单线态氧量子产率低等缺点,因此开发高效的、近红外光激发的光敏剂具有重要的研究意义。赵健/苟少华团队长期从事近红外光敏剂的研究。近年来,在新型近红外光敏剂的研究方面取得了一系列创新成果:开发了可被近红外光激活的具有D-A结构的金属钌(II)和铱(III)配合物(Nat. Commun., 2022, 13, 3064; Mater. Today. Nano., 2022, 18, 100220; Adv. Funct. Mater., 2021, 31, 2008325); 具有光激活化疗功能的钌(II)配合物(Chem. Sci., 2021, 12, 11810-11820);基于上转换材料激发的铱(III)配合物 (Small, 2020, 16, 20003633)。另外,还开发了基于苝酰亚胺结构的近红外光敏剂(ACS Materials Lett., 2023, 5, 1752-1759; ACS Materials Lett., 2022, 4, 657-664)。
近日,团队与南京大学生命分析化学国家重点实验室夏兴华教授合作,提出了一种简单可行的提高近红外光敏剂光动力效果的策略,通过自组装诱导激子-振动去耦来抑制近红外光敏剂的非辐射振动失活过程,从而克服近红外光敏剂单线态氧生成效率低的缺点,提高其光学治疗效果。根据这个思路,我们制备了两个铱(III)光敏剂,并通过理论计算和瞬态光谱等实验手段辅证了这一过程。合成的铱(III)光敏剂在体外和体内抗肿瘤试验中均表现出较好的光学治疗效果。本研究提出了一种简便有效的提高近红外金属光敏剂光敏活性的方法,对设计高效的、组织穿透深度强的近红外光敏剂具有一定的指导意义。
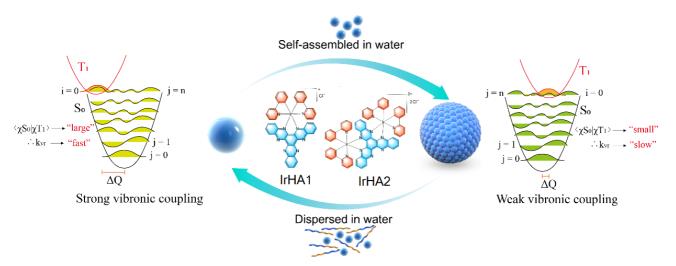
相关成果发表以“Design of Near-Infrared-Triggered Metallo-Photosensitizers via a Self-Assembly-Induced Vibronic Decoupling Strategy”为题发表于J. Am. Chem. Soc. (DOI: 10.1021/jacs.3c01645)。化学化工学院赵健副教授为论文第一作者,东南大学徐刚老师、苟少华教授和南京大学夏兴华教授为论文的共同通讯作者,东南大学为第一通讯单位。该研究工作得到了国家自然科学基金、江苏省生物药物高技术研究重点实验室及生命分析化学国家重点实验室的支持。
论文链接:https://pubs.acs.org/doi/full/10.1021/jacs.3c01645.
供稿:化学化工学院
(责任编辑:唐瑭 审核:宋业春)
























