【东大新闻网1月10日电】(通讯员 汤玉琪)近日,东南大学智能材料研究院院长、首席科学家、化学化工学院李全团队在肿瘤光免疫治疗领域取得重要进展。相关成果以“A self-assembling nanoplatform for pyroptosis and ferroptosis enhanced cancer photoimmunotherapy”(用于焦亡和铁死亡增强癌症光免疫疗法的自组装纳米平台)为题在线发表在国际权威学术期刊《Light: Science & Applications》上。东南大学硕士研究生王志超为本文第一作者,东南大学李全和汤玉琪博士为论文共同通讯作者。
免疫抑制的肿瘤微环境和肿瘤细胞低的免疫原性导致目前开发的纳米平台的免疫治疗效果并不理想。而焦亡和铁死亡,作为两种典型的免疫原性细胞死亡形式,已被证明可以激活或调节免疫系统。然而,现有的细胞焦亡和铁死亡介导的免疫治疗主要依赖化疗药物,但耐药性和毒副作用问题限制了其临床应用。因此,开发一种能高效引发肿瘤细胞焦亡和铁死亡的双功能诱导剂联合免疫佐剂来增强光免疫治疗的纳米平台,将有利于癌症光免疫治疗领域的进一步发展。
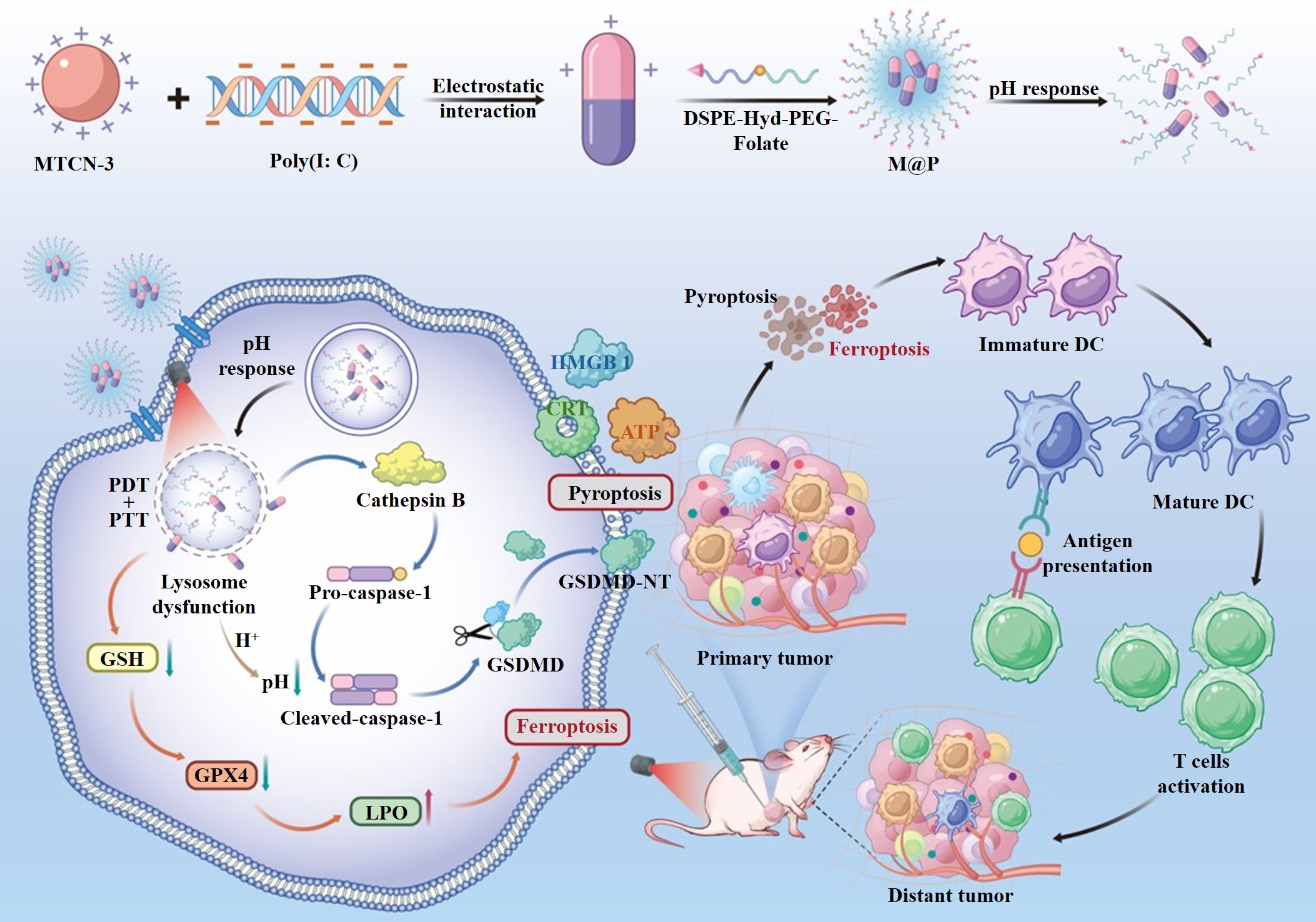
图1. 多功能纳米平台实现癌症光免疫治疗的过程。
光免疫治疗是一种结合光疗法和免疫疗法的新型癌症治疗方法。这种方法不仅可以直接杀伤肿瘤细胞,还能促使肿瘤细胞释放肿瘤相关抗原,激发全身抗肿瘤免疫应答,抑制肿瘤复发和转移。一直以来,李全团队聚焦于肿瘤光免疫治疗的研究。在前期研究 (Adv. Mater. 2023, 35, 2300232; Adv. Mater. 2025, 37, 2416122;Adv. Funct. Mater. 2024, 34, 2314832; Adv. Funct. Mater. 2024, 34, 2405367; Adv. Funct. Mater. 2025, 35, 2416359等) 的基础上, 李全团队构建了一种溶酶体靶向的pH响应的光诱导肿瘤细胞焦亡和铁死亡双功能诱导剂联合免疫佐剂的光免疫治疗纳米平台。该纳米平台可以主动靶向肿瘤细胞,并在肿瘤细胞的溶酶体中积累。在溶酶体的酸性环境中,纳米平台崩解,释放出其中的光敏剂和免疫佐剂。光敏剂在光照作用下产生大量活性氧和热量,导致溶酶体功能障碍并触发肿瘤焦亡和铁死亡。同时,这一过程配合免疫佐剂进一步激活全身性抗肿瘤免疫应答,实现光免疫治疗效果。
该研究工作得到了江苏省“双创团队”计划等项目的资助。
论文链接:https://www.nature.com/articles/s41377-024-01673-1
供稿:化学化工学院
(责任编辑:刘明源 审核:李小男)
























